Luigiego Ricciardiego 1 , Rosa Mazzeo 2,* © , Anioł Raffaele Marcotrigiano 1 , Guglielmo Rainaldiego 3 , Paolo Iovieno 4 , Vito Zonno 1 , Stefano Pavan 1 © i Concetta Lotti 2,*
- 1 Wydział Nauk o Glebie, Roślinach i Żywności, Zakład Genetyki Roślin i Hodowli Uniwersytetu w Bari, Via Amendola 165/A, 70125 Bari, Włochy; luigi.ricciardi@uniba.it (LR);angelo.marcotrigiano@uniba.it (RAMIĘ); vito.zonno@uniba.it (VZ); stefano.pavan@uniba.it (SP)
- 2 Department of Sciences of Agriculture, Food and Environment, University of Foggia, Via Napoli 25, 71122 Foggia, Włochy
- 3 Wydział Nauk Biologicznych, Biotechnologii i Biofarmaceutyków, Uniwersytet w Bari, Via Orabona 4, 70125 Bari, Włochy; guglielmo.rainaldi@uniba.it
- 4 Department of Energy Technologies, Bioenergy, Biorefinery and Green Chemistry Division, ENEA Trisaia Research Center, SS 106 Ionica, km 419+500, 75026 Rotondella (MT), Włochy; paolo.iovieno@enea.it
* Korespondencja: rosa.mazeo@unifg.it (RM); concetta.lotti@unifg.it (CL)
Abstrakcyjny:
Cebula (Allium cepa L.) jest drugą co do ważności uprawą warzyw na świecie i jest powszechnie ceniona ze względu na swoje właściwości zdrowotne. Pomimo dużego znaczenia gospodarczego i wartości jako żywności funkcjonalnej, cebula została słabo zbadana pod względem różnorodności genetycznej. Tutaj zbadaliśmy zmienność genetyczną „Cebula czerwona Acquaviva” (ARO), rasa krajowa o stuletniej historii uprawy w małym miasteczku w prowincji Bari (Apulia, południowe Włochy). Do zbadania zmienności genetycznej w kolekcji plazmy zarodkowej składającej się z 11 populacji ARO i trzech powszechnych typów komercyjnych wykorzystano zestaw 13 markerów mikrosatelitarnych. Analizy struktury genetycznej metodami parametrycznymi i nieparametrycznymi wykazały, że ARO reprezentuje dobrze zdefiniowaną pulę genów, wyraźnie odmienną od ras lądowych Tropea i Montoro, z którymi często się myli. W celu opisu bulw, zwykle używanych do spożycia świeżego, oceniono zawartość rozpuszczalnych substancji stałych i ostrość, wykazując wyższą słodycz w ARO w odniesieniu do dwóch wyżej wymienionych ras lądowych. Ogólnie rzecz biorąc, niniejsze badanie jest przydatne dla przyszłej waloryzacji ARO, która mogłaby być promowana za pomocą znaków jakości, które mogłyby przyczynić się do ograniczenia oszustw handlowych i zwiększenia dochodów drobnych posiadaczy.
Wprowadzenie
Rodzaj Allium obejmuje około 750 gatunków [1], wśród których jednym z najbardziej rozpowszechnionych jest cebula (Allium cepa L., 2n = 2x =16). A. cepa ma cykl dwuletni i przekracza zachowania reprodukcyjne. Obecnie światowa produkcja cebuli (97.9 Mt) czyni ją drugą najważniejszą uprawą warzyw po pomidorze [2]. Cebule cebulowe od dawna wykorzystywane są zarówno jako żywność, jak i w ludowych zastosowaniach leczniczych. Rzeczywiście, starożytni Egipcjanie donosili już o kilku formułach terapeutycznych opartych na wykorzystaniu czosnku i cebuli w medycznym papirusie z 1550 rpne, Codex Ebers [3].
To wszechstronne i zdrowe warzywo jest spożywane na surowo, świeże lub jako produkt przetworzony i wykorzystywane do wzmocnienia smaku wielu potraw. W kilku ostatnich badaniach stwierdzono, że spożywanie cebuli może zmniejszać ryzyko chorób sercowo-naczyniowych [4,5], otyłości [6], cukrzycy [7] i różnych form raka [8–10]. Właściwości zdrowotne cebuli są często przypisywane wysokim poziomom dwóch klas związków nutraceutycznych: flawonoidów i sulfotlenków alk(en)ylocysteiny (ACSO). Pierwsza klasa obejmuje flawonole i antocyjany. Kwercetyna jest głównym wykrywalnym flawonolem, znanym ze swoich silnych właściwości przeciwutleniających i przeciwzapalnych w wymiataniu wolnych rodników i wiązaniu jonów metali przejściowych [11]; natomiast antocyjany nadają niektórym odmianom cebuli czerwono-fioletowy kolor. Jeśli chodzi o ACSO, najobficiej występuje izoallina [(+)-trans-S-1-propenylo-L-cysteina sulfotlenek] [12], nielotny i niebiałkowy aminokwas siarkowy magazynowany w komórkach, który pośrednio odpowiada za ostry aromat i smak cebuli [13]. Po rozerwaniu tkanki izoalliina jest rozszczepiana przez enzym alliinazę z wytworzeniem szeregu lotnych związków (pirogronian, amoniak, tiosulfoniany i S-tlenek propanetialny), które wywołują łzawienie i powodują nieprzyjemny zapach (ostrość) [14]. Ostrość cebuli jest często mierzona jako ilość kwasu pirogronowego wytworzonego w wyniku hydrolizy na gram świeżej masy [1516].
W krajach basenu Morza Śródziemnego, proponowany jako jeden z drugorzędnych ośrodków różnorodności a. przecedzić [1718]cebulki cebuli charakteryzują się dużą różnorodnością kształtu, wielkości, koloru, suchej masy i ostrości [19-jeden]. Ponadto nawożenie siarką, praktyki agronomiczne, rodzaj gleby, warunki klimatyczne i genotyp odmian lub ras lokalnych mogą wpływać na jakość cebulek, nadając im szczególne wartości organoleptyczne i odżywcze [23-jeden]. We Włoszech, pomimo szerokiej dostępności plazmy zarodkowej cebuli, tylko kilka odmian cebuli jest często poddawanych badaniom naukowym i właściwie charakteryzowanym [2829].
Dokładna charakterystyka genetyczna i fenotypowa agrobioróżnorodności ma kluczowe znaczenie dla zapewnienia odpowiedniej ochrony zasobów genetycznych roślin i promowania stosowania określonych genotypów w łańcuchu wartości [30-jeden]. Do mapowania często wybierano markery prostych powtórzeń sekwencji (SSR) [33-jeden], odciski palców DNA i dyskryminacja odmian [36-jeden], oraz wiarygodne oszacowanie zmienności genetycznej w obrębie i wśród ras lądowych [39-jeden], ponieważ są one specyficzne dla locus, wieloallelowe, dziedziczone wspólnie, wysoce powtarzalne i odpowiednie do automatycznego genotypowania.
W niniejszym badaniu skupiliśmy naszą uwagę na tradycyjnej odmianie apulijskiej „Acquaviva czerwona cebula” (ARO), która jest uprawiana zgodnie z metodami rolnictwa ekologicznego na niewielkim obszarze miasta Acquaviva delle Fonti, w prowincji Bari. (Apulia, południowe Włochy). Cebule tej rasy są duże, spłaszczone i czerwone i są szeroko stosowane w lokalnych przepisach. Chociaż ARO uzyskało znak jakości „Slow Food Presidium”, jego produkcję można by dalej promować i chronić znakami jakości Unii Europejskiej, takimi jak chronione oznaczenie geograficzne (PGI) i chroniona nazwa pochodzenia (POD), ponieważ mogą one przyczynić się do ograniczenia oszustw handlowych i poprawy dochodów drobnych rolników. W tym przypadku markery molekularne SSR wykorzystano jako potężne narzędzia do oceny zmienności genetycznej wśród populacji ARO i do odróżnienia tej rasy lokalnej od pozostałych dwóch południowych włoskich odmian czerwonej cebuli. Ponadto oszacowaliśmy ostrość i zawartość rozpuszczalnych substancji stałych, aby ocenić smak ARO w odniesieniu do zapotrzebowania rynku.
Efekt
Założenie kolekcji plazmy zarodkowej Acquaviva z czerwonej cebuli i charakterystyka morfologiczna
Do stworzenia kolekcji plazmy zarodkowej ARO wykorzystano nasiona 13 populacji rasy ARO, przekazane przez rolników w ramach projektu BiodiverSO Apulia Region.
Deskryptory morfologiczne, związane z cebulą, skórą i miąższem, zostały zebrane na plazmie zarodkowej ARO i na trzech lokalnych odmianach cebuli, z których dwie należą do rasy „Tropea czerwona cebula” (TRO) i jedna do „Montoro miedziana cebula” (MCO) (ryc. 1). Wszystkie cebulki ARO były płaskie i charakteryzowały się czerwoną skórką zewnętrzną oraz miąższem o różnych odcieniach czerwieni. Natomiast miąższ cebulek TRO był całkowicie czerwony, podczas gdy miąższ cebulek MCO był słabo pigmentowany (tabela S1). Analiza biochemiczna pozwoliła na ocenę zawartości substancji rozpuszczalnych i ostrości. Jak podano w tabeli 1, Średnia zawartość substancji rozpuszczalnych w bulwach w populacjach ARO wynosiła 7.60 i wahała się od 6.00 (ARO12) do 9.50° Brixa (ARO11 i ARO13). Wartość ta była wyższa niż oszacowana dla ras lądowych TRO i MCO (odpowiednio 4.25 i 6.00° Brixa).

Tabela 1. Zawartość substancji stałych rozpuszczalnych i wartości ostrości oceniane w populacjach „Acquaviva Red Onion” (ARO), „Tropea Red Onion” (TRO) i „Montoro Copper Onion” (MCO) *.
| KOD | Rozpuszczalna zawartość substancji stałych (Brix) | Ostrość (pmolg-1 FW) | ||
| Oznaczać | CV y (%) | Oznaczać | CV y (%) | |
| ARO1 | 6.25 D * | 5.65 | 5.84 od * | 23.78 |
| ARO2 | 7.25 DC | 4.87 | 6.51 | 22.98 |
| ARO3 | 7.50 BCD | 9.42 | 5.28 rok | 22.88 |
| ARO4 | 7.50 BCD | 0.00 | 6.97 | 3.74 |
| HOOP 5 | 7.50 BCD | 0.00 | 6.80 | 9.68 |
| ARO6 | 6.25 D | 5.65 | 4.51 rok | 39.18 |
| ARO7 | 7.25 DC | 4.87 | 5.25 rok | 15.44 |
| ARO8 | 9.00 AB | 0.00 | 7.04 | 3.49 |
| ARO9 | 8.25 ABC | 4.28 | 6.84 | 0.15 |
| ARO10 | 7.00 DC | 0.00 | 5.94 rok | 6.57 |
| ARO11 | 9.50 | 7.44 | 5.54 rok | 16.43 |
| ARO12 | 6.00 D | 0.00 | 4.91 rok | 9.70 |
| ARO13 | 9.50 | 7.44 | 6.63 | 24.93 |
| MCO | 6.00 D | 0.00 | 4.18 rok | 2.66 |
| TRO1 | 4.25 E | 8.31 | 2.80 b | 2.10 |
| TRO2 | 4.25 E | 8.31 | 4.28 rok | 4.79 |
* Średnie z tymi samymi literami wielkimi lub małymi nie różnią się statystycznie odpowiednio przy 0.01P lub 0.05P (Test SNK). y Współczynnik zmienności.
Średnia wartość ostrości ARO, oceniona za pomocą zawartości kwasu pirogronowego, wyniosła 6.00, wahała się od 4.51 pmol g-1 FW (ARO6) do 7.04 (ARO8). Wartość ta była wyższa niż oszacowana w rasach lądowych TRO i MCO (3.54 pmol g-1 FW i 4.18 pmol g-1 FW).
Polimorfizm SSR i zależności genetyczne między akcesją
W niniejszym badaniu 11 z 37 testowanych kombinacji starterów SSR dostarczyło polimorfizmów pojedynczego locus, tj. dało co najwyżej dwa produkty amplifikacji u jednego osobnika. Ogólnie 55 alleli wykryto u 320 osób z liczbą alleli na locus w zakresie od 2 (ACM147 i ACM 504) do 11 (ACM132) i średnią wartością 5 alleli (Tabela 2). W poszczególnych populacjach liczba alleli (Na) wahała się od 1.94 (ACM147 i ACM504) do 5.38 (ACM132), natomiast efektywna liczba alleli (Ne) wahała się od 1.41 (ACM152) do 2.82 (ACM449). Rozbieżności pomiędzy wartościami Na i Ne wynikały z obecności alleli o niskiej częstości występowania w populacjach i przewagi zaledwie kilku alleli. Najwyższą obserwowaną wartość heterozygotyczności (Ho) podkreślono dla ACM138 i ACM449 (0.62), natomiast najniższą powiązano z ACM152 (0.25). Oczekiwana heterozygotyczność (He), która odpowiada teoretycznemu oczekiwaniu w populacji panmiktycznej, wahała się od 0.37 (ACM504) do 0.61 (ACM132, ACM138 i ACM449). Wskaźnik fiksacji Wrighta (Fis) wykazał wartości bliskie zeru (średnia 0.05) dla wszystkich markerów, wskazując na podobne wartości między obserwowanymi i oczekiwanymi poziomami heterozygotyczności, jak oczekiwano dla gatunków krzyżujących się. Skuteczność pojedynczego markera SSR w genetycznym odcisku palca oszacowano za pomocą wskaźnika polimorficznej zawartości informacji (PIC), o średniej wartości 0.48 i wahającej się od 0.33 (ACM504) do 0.67 (ACM132). Inny wskaźnik sprawności, wskaźnik informacyjny Shannona (I), wykazywał średnią wartość 0.84, a zakładane wartości wahały się od 0.45 (ACM152) do 1.20 (ACM132).
Tabela 2. Cechy polimorfizmu 11 markerów SSR używanych do szacowania różnorodności genetycznej w populacjach ARO, TRO i MCO. Całkowita liczba alleli (Na), zakres wielkości prążków i indeks zawartości informacji polimorficznych (PIC) Odnieś się do całkowitego zestawu 320 osobników genotypowanych w tym badaniu. Liczba alleli (Na), liczba alleli efektywnych (Ne), obserwowana heterozygotyczność (Ho), oczekiwana heterozygotyczność (He), wskaźnik fiksacji (Fis), a wskaźnik informacyjny Shannona (I) odnosi się do średnich wartości obliczonych z 16 populacji, z których każda składa się z 20 osobników.
| Umiejscowienie. | Suma Na | Zakres rozmiarów (pz) | PIC | Oznaczać | |||||
| Na | Ne | Ho | He | I | Fis | ||||
| ACM91 | 4 | 189-205 | 0.40 | 2.63 | 1.72 | 0.38 | 0.39 | 0.66 | 0.04 |
| ACM101 | 4 | 229-241 | 0.52 | 2.94 | 2.37 | 0.53 | 0.56 | 0.92 | 0.06 |
| ACM132 | 11 | 186-248 | 0.67 | 5.38 | 2.78 | 0.55 | 0.61 | 1.20 | 0.09 |
| ACM138 | 5 | 242-272 | 0.66 | 3.69 | 2.82 | 0.62 | 0.61 | 1.09 | -0.02 |
| ACM147 | 2 | 264-266 | 0.37 | 1.94 | 1.83 | 0.44 | 0.44 | 0.62 | -0.01 |
| ACM152 | 4 | 228-244 | 0.25 | 2.38 | 1.41 | 0.25 | 0.27 | 0.45 | 0.07 |
| ACM235 | 4 | 286-298 | 0.41 | 2.81 | 1.77 | 0.44 | 0.41 | 0.72 | -0.06 |
| ACM446 | 6 | 108-120 | 0.56 | 3.50 | 2.48 | 0.49 | 0.58 | 1.01 | 0.16 |
| ACM449 | 8 | 120-140 | 0.66 | 4.88 | 2.82 | 0.62 | 0.61 | 1.18 | -0.03 |
| ACM463 | 5 | 202-210 | 0.47 | 3.38 | 1.95 | 0.46 | 0.48 | 0.83 | 0.05 |
| ACM504 | 2 | 188-192 | 0.33 | 1.94 | 1.64 | 0.30 | 0.37 | 0.54 | 0.20 |
| Oznaczać | 5 | 0.48 | 3.22 | 2.15 | 0.46 | 0.48 | 0.84 | 0.05 |
Wśród populacji ARO3, ARO6, ARO8, ARO10, TRO1 i MCO wykazywały wysoki poziom zmienności genetycznej (Ho > 0.5), natomiast najmniejsze zróżnicowanie zaobserwowano w populacji ARO7 (Ho = 0.27) (Tabela uzupełniająca S2). Ogólnie rzecz biorąc, wszystkie przystąpienia wyświetlane Fis wartości bliskie zeru (Fis średnia wartość = 0.054), jak oczekiwano w losowych warunkach kojarzenia.
Analiza wariancji molekularnej i struktury genetycznej
Hierarchiczny podział zmienności genetycznej pomiędzy populacjami iw obrębie populacji został obliczony przez AMOVA. Wyniki wskazały na znaczną część zmienności genetycznej w populacjach (87%). Zróżnicowanie między populacjami, 13%, było bardzo istotne (P < 0.001) (Tabela 3). Wartości parami parametru Fpt, analogicznego do wskaźnika fiksacji Fst Wrighta, w zakresie od 0.002 (ARO2/ARO10) do 0.468 (ARO7/TRO2), były istotne (P < 0.05), z wyjątkiem dziewięciu porównań parami (tabela uzupełniająca S3).
Tabela 3. Analiza wariancji molekularnej 320 genotypów z 16 populacji Allium cepa L.
| Źródło | df | Suma kwadratów | Szacowanie wariancji | Wariancja (%) | Fpt | P |
| Wśród populacji | 15 | 458.63 | 1.16 | 13% | ||
| W obrębie populacji | 304 | 2272.99 | 7.50 | 87% | 0.134 | 0.001 |
| Kwota produktów: | 319 | 2731.62 | 8.66 |
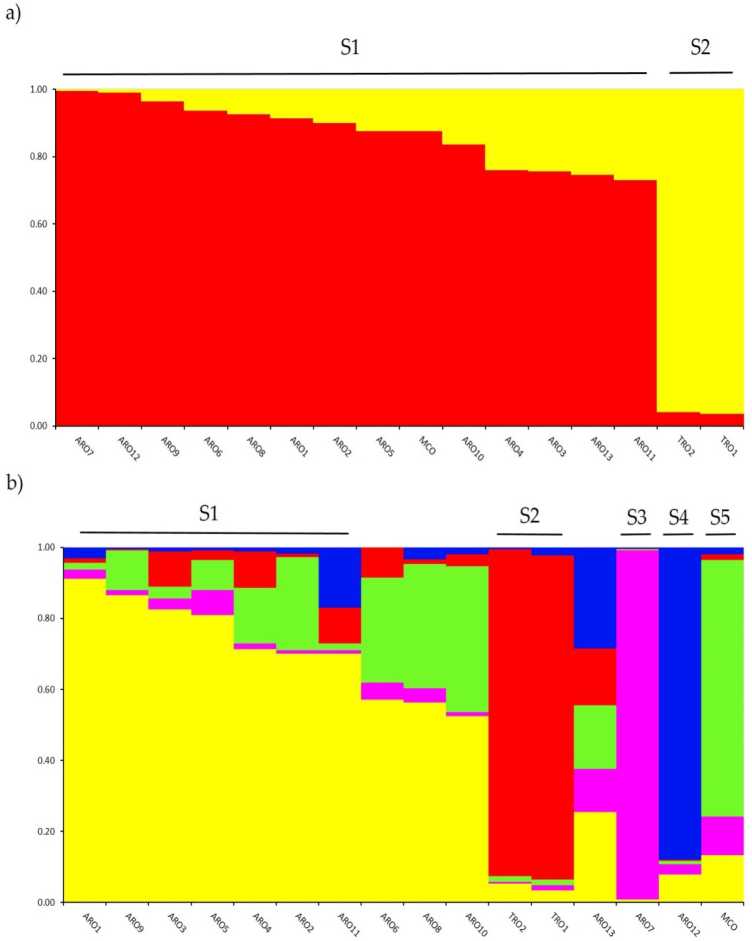
Badanie struktury genetycznej w a. przecedzić genotypowany w niniejszym badaniu zbiór został wykonany za pomocą analizy skupień opartej na modelu domieszki zaimplementowanej w oprogramowaniu STRUCTURE. Metoda Evanno AK zasugerowała podział na dwa skupienia (K = 2) jako najbardziej informacyjny dla naszego zestaw danych,z THe Następny najwyższy peak w K = 5 (suplementaiv Rgure S1), ZA widelec = 2, ahpopwnigdzie dupieigned teżnof dwa klastry w współczynnik rnernbertoip (q) > 0.7. Jak showygrać w Postać 2a, pierwszy klaster (o nazwie S1) obejmował MCO i wszystkie populacje ARO, podczas gdy klaster S2 grupował dwie populacje TRO. Przy K = 5, zapewniając głębszy opis zbioru danych (rysunek 2b), 75% przystąpień przypisano do jednego z pięciu klastrów. Potwierdzono rozdział między ARO (S1) i TRO (S2), chociaż niektóre populacje ARO zostały zmieszane (q < 0.7) lub zgrupowane oddzielnie w dwóch nowych klastrach S3 i S4 (odpowiednio ARO7 i ARO12). Co ciekawe, komercyjny typ MCO utworzył wyraźną gromadę (S5) oddzieloną od czerwonej cebuli apulijskiej.
Związki genetyczne między populacjami
Polimorfizm SSR pozwolił na sporządzenie dendrogramu różnorodności genetycznej, a wyniki analizy filogenetycznej przedstawiono na ryc. 3a. Tutaj kolekcja plazmy zarodkowej została podzielona na pięć grup silnie wspieranych przez wartości bootstrap. Populacje ARO7 i ARO12 zostały natychmiast oddzielone od pozostałych populacji i utworzyły dwa odrębne klastry. Trzeci klaster obejmował dwie komercyjne populacje TRO, podczas gdy czwarty węzeł dzielił MCO od jedenastu populacji ARO. Związek genetyczny występujący między populacjami był dalej badany za pomocą analizy głównych współrzędnych (PCoA) (ryc 3b). Jak już wcześniej podkreślono, populacje ARO zostały zgrupowane ciasno, z wyjątkiem ARO12 i ARO7, które pojawiły się w izolowanych pozycjach na wykresie PCoA. Dwie populacje TRO i MCO były rozproszone w prawym dolnym panelu wykresu.
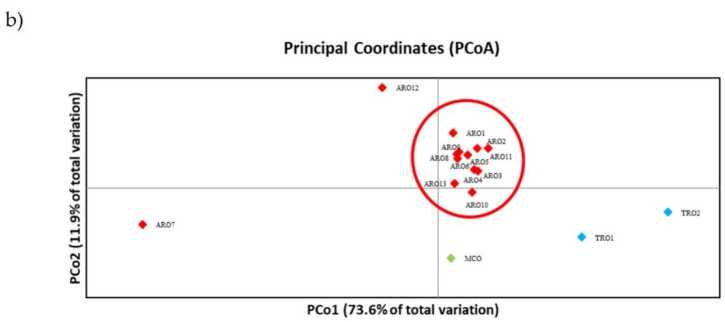
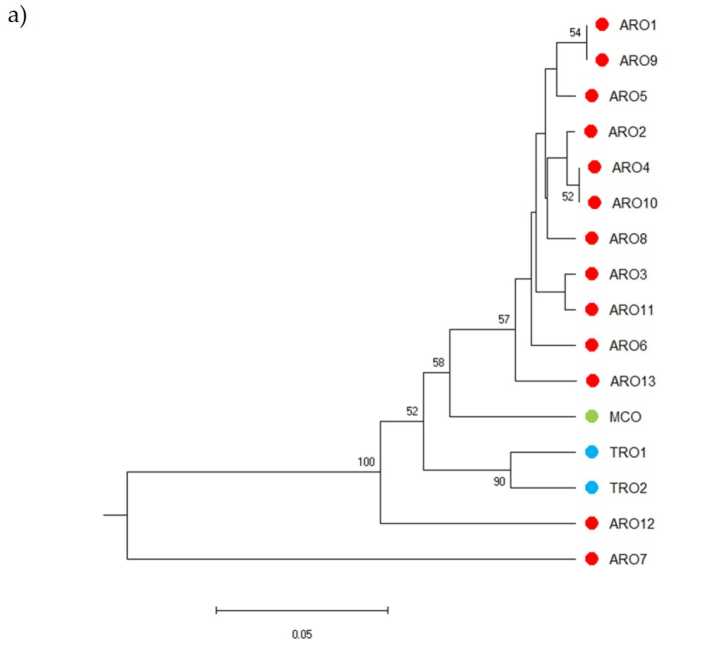
Rysunek 3. Różnorodność genetyczna wśród 16 a. przecedzić populacje scharakteryzowane w tym badaniu, na podstawie ich profilu SSR. (a) Dendrogram UPGMA dystansu genetycznego. Wartości wsparcia Bootstrap >50 są wskazane powyżej odpowiednich węzłów; (b) analiza głównych składowych (PCoA). Klaster zakreślony na czerwono w pełni pasował do grupy wygenerowanej przez analizę filogenetyczną i składał się z 11 przyłączeń ARO.
Dyskusja
W ramach dużej agro-bioróżnorodności tradycyjnie uprawianej w południowych Włoszech, odmiany cebulowe stanowią produkty niszowe, które należy chronić przed ryzykiem erozji genetycznej i zastąpieniem przez nowoczesne odmiany. W ramach regionalnego projektu BiodiverSO, którego celem jest gromadzenie, charakterystyka, promocja i ochrona zasobów genetycznych regionu Apulia silnie związanych z lokalnym dziedzictwem, utworzyliśmy kolekcję nasion 13 populacji rasy ARO. Przedstawiliśmy pierwszą ocenę zmienności ARO pod względem polimorfizmu DNA i dwóch parametrów biochemicznych, zawartości rozpuszczalnej substancji stałej i kwasu pirogronowego, związanych z cechami smakowymi i znaczeniem dla akceptacji świeżych produktów surowych. Ponadto dane dotyczące rasy ARO zostały porównane z danymi zebranymi na temat dwóch innych ras lokalnych cebuli pigmentowanej, z którymi często się mylił.
Analizy biochemiczne wykazały słodycz 13 populacji ARO, związaną z wysoką zawartością rozpuszczalnych substancji stałych i średnią ostrością, zgodnie z wytycznymi przemysłu słodkiej cebuli [31]. Żarówki ARO były słodsze niż odmiany TRO i MCO i wykazywały nieco większą ostrość. Jednak słodycz cebuli wynika z równowagi między zawartością cukru a ostrością, dlatego ta charakterystyka może być użyteczna we wspieraniu wyboru genotypów wartości, zwykle dokonywanej przez rolników wyłącznie na podstawie morfologii.
Potwierdzono, że markery SSR są użytecznym narzędziem do rozróżniania genotypów, aczkolwiek zbierane na wąskim obszarze upraw, takim jak miasto Acquaviva delle Fonti. Wybrane markery wykazywały większą liczbę alleli niż markery wcześniej raportowane przez [43] i [44], ale niższy niż wskaźniki zgłoszone przez [45]. Co więcej, 50% naszego zestawu markerów wykazywało wartości wskaźnika PIC większe niż 0.5, co okazało się odpowiednie do rozróżniania populacji w kolekcji, jak sugeruje [46]. Ocena zróżnicowania w obrębie populacji wykazała podobne wartości między Ho i He, co skutkuje niskim Fis wartości. Jest to zgodne z przekrojową naturą A. cepa, która poważnie cierpi na depresję inbredową [47]. Ogólna Fis wartość obliczona w populacjach cebuli uwzględnionych w tym badaniu (0.054) była niższa niż ta podana wcześniej przez [45] (0.22) i prawie identyczny z tym znalezionym przez [31] (0.08) i [48] (0.00), którzy ocenili różnorodność genetyczną lokalnych odmian cebuli odpowiednio z północno-zachodniej Hiszpanii i Nigru. Godne uwagi poziomy heterozygotyczności w populacjach ARO potwierdzają pogląd, że Apulia reprezentuje centrum różnorodności dla wielu gatunków ogrodniczych [32, 42, 49-jeden].
AMOVA podkreśliła, że większość zmienności molekularnej w kolekcji genotypowanej w tym badaniu dotyczy populacji. Jednak znaczące zróżnicowanie genetyczne między populacjami (FPT wartości) ujawniły występowanie stratyfikacji genetycznej. W rzeczywistości, chociaż nasze wyniki wskazywały na obecność jednorodności genetycznej w większości populacji ARO, tworzących dobrze zdefiniowany klaster, populacje ARO7 i ARO12 wykazywały wyraźnie odrębny profil genetyczny. Wynik ten mógł wynikać z innego pochodzenia nasion wykorzystywanych przez dwóch rolników, od których zebrano populacje. Ponadto, na podstawie uzyskanych wyników, rasę krajową ARO można uznać za wyraźnie odmienną na poziomie genetycznym od ras lądowych TRO i MCO. W niedawnym badaniu [29] ocenił różnorodność genetyczną kilku włoskich odmian cebuli, w tym „Acquaviva”, „Tropea” i „Montoro”. Chociaż autorzy wykorzystali markery SNP do oceny różnorodności genetycznej szerszej kolekcji cebuli, genotypowanie nie było w stanie odróżnić cebuli „Acquaviva” od „Tropea” i „Montoro”. Prawdopodobnie rozbieżność ta wynika z niskiej średniej znalezionej wartości PIC (0.292), co sugeruje skromną ogólną informacyjność analizowanych loci, jak twierdzi [29]. Ponadto, w celu zbadania obecności podstruktury w ich włoskim klastrze, lepiej byłoby przeanalizować włoskie genotypy oddzielnie od reszty kolekcji. Prawdopodobnie pozwoliłoby to na wizualizację wzorca różnorodności genetycznej powiązanej ze stratyfikacją geograficzną lub cechami podlegającymi selekcji empirycznej.
Podsumowując, niniejsze badanie stanowi obszerny raport na temat uprawy cebuli związanej z lokalnym dziedzictwem kulturowym i mającej znaczenie gospodarcze dla rolników. Nasze wyniki podkreślają, że z kilkoma wyjątkami ARO charakteryzuje się dobrze zdefiniowaną pulą genów, która zasługuje na ochronę przed ryzykiem erozji genetycznej. Dlatego kluczowe było utworzenie reprezentatywnej kolekcji tego cennego źródła różnorodności genetycznej. Wreszcie charakterystyka genetyczna i fenotypowa ARO może być przydatna do uzyskania znaków jakości z Unii Europejskiej.
Materiały i Metody
Pobieranie plazmy zarodkowej, materiał roślinny i ekstrakcja DNA
Zestaw 13 populacji rasy ARO został pozyskany w ramach projektu regionu Apulia (BiodiverSO: https://www.biodiversitapuglia.it/), poprzez szereg misji realizowanych w “Acquaviva delle Fonti”, małym miasteczku w Apulii w prowincji Bari we Włoszech. Miejsca zbierania każdego dostępu zostały zmapowane za pomocą Systemu Informacji Geograficznej (GIS) i przedstawione w Tabeli 4. Ponadto w niniejszym badaniu uwzględniono dwie populacje z rasy TRO i jedną populację z rasy MCO i wykorzystano jako odniesienie. Cały materiał roślinny był uprawiany w tych samych warunkach środowiskowych na farmie doświadczalnej “P Martucci” Uniwersytetu w Bari (41° 1'22.08″ N, 16°54'25.95″ E), pod klatką ochronną, aby uniknąć zapylenia krzyżowego populacje i zapewnienie wewnątrzpopulacyjnego zapylenia za pomocą much plujkowych (Cezar Lucilii). 16 populacji scharakteryzowano pod kątem cech związanych z wielkością i kształtem bulw oraz kolorem skóry i miąższu (tabela S1). Dodatkowo wykonano oznaczenie zawartości części stałych rozpuszczalnych za pomocą ręcznego refraktometru i zmierzono ostrość w próbkach soku cebulowego z dodatkiem 2,4-dinitrofenylohydrazyny (0.125% v/v w 2N HCl) i oceniając absorbancję przy 420 nm, jak donosi [31]. W celu określenia obecności istotnych różnic przeprowadzono test wielozakresowy Duncana i test SNK.
Tabela 4. Lista populacji zebranych i genotypowanych w tym badaniu. Dla każdej populacji raportowany jest kod identyfikacyjny, nazwa lokalna, współrzędna GPS i bank genów zabezpieczający nasiona.
| Code | Imię | Współrzędne GPS | Bank Genów y |
| ARO1 | Cipolla Rossa di Acquaviva | 40°54’21.708″ N 16°49’1.631” E | Di.SSPA |
| ARO2 | Cipolla Rossa di Acquaviva | 40°53’14.28″ N 16°48’56.879” E | Di.SSPA |
| ARO3 | Cipolla Rossa di Acquaviva | 40°54’11.304″ N 16°49’13.079” E | Di.SSPA |
| ARO4 | Cipolla Rossa di Acquaviva | 40°54’3.348″ N 16°40’27.011” E | Di.SSPA |
| ARO5 | Cipolla Rossa di Acquaviva | 40°51’59.76″ N 16°53’0.527” E | Di.SSPA |
| ARO6 | Cipolla Rossa di Acquaviva | 40°52’48.72″ N 16°49’43.247” E | Di.SSPA |
| ARO7 | Cipolla Rossa di Acquaviva | 40°53’13.47″ N 16°50’23.783” E | Di.SSPA |
| ARO8 | Cipolla Rossa di Acquaviva | 40°53’18.816″ N 16°49’33.888” E | Di.SSPA |
| ARO9 | Cipolla Rossa di Acquaviva | 40°54"51.372 "N 16"°49"3.504" E | Di.SSPA |
| ARO10 | Cipolla Rossa di Acquaviva | 40°54’1.188″ N 16°49’24.311” E | Di.SSPA |
| ARO11 | Cipolla Rossa di Acquaviva | 40°52"49.8 "N 16"°49"48.575" E | Di.SSPA |
| ARO12 | Cipolla Rossa di Acquaviva | 40°52’38.892″ N 16°49’28.379” E | Di.SSPA |
| ARO13 | Cipolla Rossa di Acquaviva | 40°53’21.768″ N 16°49’29.711” E | Di.SSPA |
| TRO1 | Cipolla rossa luga w Tropei | - | Di.SSPA |
| TRO2 | Cipolla rossa tonda w Tropei | - | Di.SSPA |
| MCO | Cipolla Ramata di Montoro | - | Di.SSPA |
| y Di.SSPA, Wydział Nauk o Glebie, Roślinach i Żywności, Uniwersytet w Bari. |
Materiał liści o 20 genotypach na populację pobrano i przechowywano w temperaturze -80 °C do czasu użycia. Dla gatunków bogatych w polisacharydy, jak A. cepa, pierwsze kroki w celu usunięcia polisacharydu są niezbędne do uzyskania dobrej jakości DNA, dlatego wstępne płukania w buforze STE (0.25 M sacharozy, 0.03 M Tris, 0.05 M EDTA) przeprowadzono zgodnie z opisem [52]. Całkowite DNA zostało wyekstrahowane zgodnie z metodą CTAB [53] i na koniec sprawdzono jakość i stężenie za pomocą spektrofotometru Nano Drop 2000 UV-vis (ThermoScientific, Waltham, MA, USA) i elektroforezy w 0.8% żelu agarozowym.
Analiza SSR
16 kombinacji starterów EST-SSR opracowanych przez [54] i wcześniej przetestowany w badaniach różnorodności genetycznej przez [43] i [44] i 21 genomowych SSR [45-jeden] zostały przebadane w celu oceny ich przydatności (tabela uzupełniająca S4). Genotypowanie przeprowadzono przy użyciu ekonomicznej metody znakowania fluorescencyjnego, w której ogon M13 jest dodawany do każdego startera przedniego SSR [56]. Mieszanki PCR przygotowano w reakcji 20 gL zawierającej: 50 ng całkowitego DNA, 0.2 mM mieszanki dNTP, 1X buforu do reakcji PCR, 0.8 U polimerazy DNA DreamTaq (Thermo Scientific, Waltham, MA, USA), 0.16 gM startera wstecznego , 0.032 gM startera do przodu wydłużonego o sekwencję M13 (5'-TGTAAAACGACGGCCAGT-3') i 0.08 gM uniwersalnego startera M13 znakowanego barwnikami fluorescencyjnymi FAM lub NED (Sigma-Aldrich, St. Louis, MO, USA). Reakcje PCR przeprowadzono w termocyklerze SimpliAmp (Applied Biosystems, CA, USA) w następujących warunkach dla większości par starterów: 94°C przez 5 min, 40 cykli w 94°C przez 30 s, 58°C przez 45 s i 72°C przez 45 s i końcowe wydłużenie w 72°C przez 5 min. Podobnie jak w przypadku ACM446 i ACM449, zastosowano reakcję PCR typu touchdown z przyłączaniem w temperaturze 60 °C do 55 °C przez 10 cykli, 30 cykli w 55 °C, a następnie końcowe wydłużanie przez 5 minut w 72 °C. Produkty PCR wprowadzono do 96-studzienkowej płytki i zmieszano z 14 µl Hi-Di Formamidu (Life Technologies, Carlsbad, CA, USA) i 0.5 µl GeneScan 500 ROX Size Standard (Life Technologies, Carlsbad, CA, USA). Amplikony rozdzielono za pomocą aparatu do sekwencjonowania kapilarnego ABI PRISM 3100 Avant Genetic Analyzer (Life Technologies, Carlsbad, CA, USA), gdzie allele oceniono jako współdominujące i przypisano przy użyciu oprogramowania GeneMapper Software w wersji 3.7.
Oprogramowanie GenAlEx 6.5 [57] i Cervus 3.0.7 [58] zostały wykorzystane do oszacowania liczby alleli (Na), liczby alleli efektywnych (Ne), obserwowanej heterozygotyczności (Ho), oczekiwanej heterozygotyczności (He), polimorficznej zawartości informacji (PIC), wskaźnika informacji Shannona (I) i wskaźnika fiksacji (Fis). ) dla każdego locus SSR.
Ocena różnorodności genetycznej
Hierarchiczny podział zmienności genetycznej między populacjami cebuli iw obrębie populacji oceniano za pomocą GenAlEx 6.5 [57] poprzez analizę wariancji molekularnej (AMOVA) z 999 bootstrapem w celu przetestowania istotności. Ponadto oprogramowanie GenAlEx 6.5 zostało użyte do oszacowania różnorodności w każdej populacji poprzez obliczenie średniej Ho, He i Fis we wszystkich loci SSR.
Struktura populacji została wywnioskowana przez algorytm grupowania oparty na modelu bayesowskim zaimplementowany w oprogramowaniu STRUCTURE v.2.3.4 [59]. Zestaw danych prowadzono z kilkoma hipotetycznymi skupieniami (K), w zakresie od 1 do 10, ustalając dziesięć niezależnych przebiegów na każdą wartość K. Dla każdego przebiegu, mając na celu zweryfikowanie zgodności wyników, przeprowadzono 100,000 100,000 początkowego okresu wypalenia i XNUMX XNUMX iteracji Markowa Łańcucha Monte Carlo (MCMC) w modelu domieszek i niezależnych częstości alleli w populacjach. Najbardziej prawdopodobną wartość K wyznaczono stosując metodę AK, opisaną przez [60], w internetowym programie STRUCTURE HARVESTER [61]. Poszczególną populację przypisywano do konkretnego skupienia, gdy jej współczynnik przynależności (wartość q) był wyższy niż 0.7, w przeciwnym razie uznawano ją za mieszaną.
Przeprowadzono analizę głównych współrzędnych w celu wizualizacji wzorców pokrewieństwa genetycznego między przynależnościami ujawnionymi przez macierz odległości genetycznej Nei (tabela uzupełniająca S5). Na podstawie częstości alleli skonstruowano dendrogram odległości genetycznej wykorzystując metodę grup nieważonych par z analizą skupień średnich arytmetycznych (UPGMA) w oprogramowaniu POPTREEW [62]. Do oceny pewności hierarchicznego grupowania zastosowano metodę bootstrapping, ustawiając 100 ponownego próbkowania zbioru danych. Wreszcie oprogramowanie MEGA X [63] był używany jako oprogramowanie do rysowania drzew.
Materiały uzupełniające: Następujące informacje są dostępne online na stronie http://www.mdpi.com/2223-7747/9/2/260/s1. Tabela S1: Charakterystyka morfologiczna żarówek ARO, MCO i TRO. Tabela S2: Wskaźniki heterozygotyczności i fiksacji obliczone dla ras lądowych ARO oraz TRO i MCO. Tabela S3: Wartości parami parametru Fpt. Tabela S4: Lista SSR użytych w badaniu. Tabela S5. Parowa macierz populacji odległości genetycznej Nei. Rysunek S1: Wykres liniowy wartości K zmieniających się wraz z Delta K Evanno.
Autorskie Wkłady: CL i LR opracowali badanie i zaprojektowali eksperyment; CL i PI wykonały analizę markerów molekularnych; ARM i VZ przeprowadziły próby terenowe; RM, SP, GR i CL byli zaangażowani w analizę danych; RM i CL napisali manuskrypt. Wszyscy autorzy przeczytali i zgodzili się na opublikowaną wersję rękopisu.
Finansowanie: Praca ta została sfinansowana przez regionalny projekt apulijski „Bioróżnorodność gatunków warzyw apulijskich”—Programma di Sviluppo Rurale per la Puglia 2014-2020. Misura 10 — Sottomisura 10.2; przyznanie CUP H92C15000270002, Włochy.
Podziękowanie: Podziękowania należą się „Azienda Agricola Iannone Anna” oraz „Associazione produttori della vera cipolla rossa di Acquaviva” za dostarczenie materiałów roślinnych użytych w eksperymencie.
Konflikt interesów: Autorzy deklarują brak konfliktu interesów.
Referencje
- 1. Stearn, WT Ile znanych jest gatunków Allium? Kew Mag. 1992, 9, 180-182. [CrossRef]
- 2. FAOSTAT. Baza danych statystycznych FAO. Dostępny online: http://www.fao.org/2017 (dostęp 8 stycznia 2019 r.).
- 3. Blok E. Chemia czosnku i cebuli. Sci. Rano. 1985, 252, 114-119. [CrossRef]
- 4. Lee, B.; Jung, JH; Kim, HS Ocena działania czerwonej cebuli na aktywność przeciwutleniającą u szczura. Chemia Spożywcza Toksykol. 2012, 50, 3912-3919. [CrossRef]
- 5. Lee, SM; Księżyc, J.; Chung, JH; Cha, YJ; Shin, MJ Wpływ ekstraktów ze skórki cebuli bogatych w kwercetynę na zakrzepicę tętniczą u szczurów. Chemia Spożywcza Toksykol. 2013, 57, 99-105. [CrossRef] [PubMed]
- 6. Yoshinari, O.; Shiojima, Y.; Igarashi, K. Efekty przeciw otyłości ekstraktu z cebuli u szczurów tłuszczowych z cukrzycą Zucker. Składniki odżywcze 2012, 4,1518-1526. [CrossRef]
- 7. Akash, MSH; Rehman K.; Chen, S. Roślina przyprawowa Allium cepa: Suplement diety do leczenia cukrzycy typu 2. Odżywianie 2014, 30, 1128-1137. [CrossRef] [PubMed]
- 8. Wang, Y.; Tian, WX; Ma, XF Hamujące działanie cebuli (Allium cepa L.) ekstrakt na proliferację komórek nowotworowych i adipocytów poprzez hamowanie syntazy kwasów tłuszczowych. Azjatycki Pac. J. Cancer Poprzedni. 2012,13, 5573-5579. [CrossRef] [PubMed]
- 9. Lai, WW; Hsu, SC; Chueh, FS; Chen, YY; Yang, JS; Lin, JP; Zastaw, JC; Tsai, CH; Chung, JG Quercetin hamuje migrację i inwazję ludzkich komórek raka jamy ustnej SAS poprzez hamowanie szlaków sygnałowych NF-kappaB i metaloproteinazy macierzy-2/-9. Przeciwnowotworowe Res. 2013, 33, 1941-1950. [PubMed]
- 10. Nicastro, HL; Ross, SA; Milner, JA Czosnek i cebula: ich właściwości profilaktyczne. Rak Poprzedni. Res. 2015, 8,181-189. [CrossRef]
- 11. Forte, L.; Torricelli, P.; Boanini, E.; Gazzano, M.; Rubini, K.; Fini, M.; Bigi, A. Właściwości przeciwutleniające i naprawcze kości hydroksyapatytu funkcjonalizowanego kwercetyną: badanie in vitro kokultury komórek osteoblastów, osteoklastów i śródbłonka. Acta Biomater. 2016, 32, 298-308. [CrossRef]
- 12. Yamazaki, Y.; Iwasaki, K.; Mikami, M.; Yagihashi, A. Dystrybucja jedenastu prekursorów smaku, pochodnych S-Alk(en)ylo-L-cysteiny, w siedmiu warzywach Allium. Nauka o żywności. Technol. Res. 2011, 17, 55-62. [CrossRef]
- 13. Block, E. Chemia organosulfur of the Genus Allium — Implikacje dla organicznej chemii siarki. Angew. Chem. wewn. Wyd. inż. 1992, 31, 1135-1178. [CrossRef]
- 14. Griffiths, G.; Trueman, L.; Crowther, T.; Tomasz B.; Smith, B. Cebula – Globalna korzyść dla zdrowia. Fitoter. Res. 2002,16, 603-615. [CrossRef]
- 15. Schwimmer S.; Weston, WJ Enzymatyczny rozwój kwasu pirogronowego w cebuli jako miara ostrości. J. Rolnictwo. Chemia Spożywcza 1961, 9, 301-304. [CrossRef]
- 16. Ketter, kot; Randle, WM Ocena ostrości w cebuli. W Testowane badania do nauczania laboratoryjnego; Karcher, SJ, wyd.; Association for Biology Laboratory Education (ABLE): Nowy Jork, NY, USA, 1998; Tom 19, s. 177-196.
- 17. Hanelt, P Taksonomia, ewolucja i historia. W Cebula i rośliny pokrewne, tom. I. Botanika, Fizjologia i Genetyka; Rabinowicz, HD, Brewster, JL, wyd.; CRC Press: Boca Raton, FL, USA, 1990; s. 1-26.
- 18. Rabinowicz, HD; Currah, L. Nauka o uprawie Allium: ostatnie postępy; Wydawnictwo CABI: Wallingford, Wielka Brytania, 2002.
- 19. Mallor, C.; Caravedo, M.; Estopanan, G.; Mallor, F. Charakterystyka zasobów genowych cebuli (Allium cepa L.) z hiszpańskiego drugorzędnego centrum różnorodności. Zakres. J. Rolnictwo. Res. 2011, 9, 144-155. [CrossRef]
- 20. Ferioli, F.; D'Antuono, LF Ocena zawartości fenoli i sulfotlenków cysteiny w miejscowej plazmie zarodkowej cebuli i szalotki z Włoch i Ukrainy. Genet. Zasob. Przytnij Evol. 2016, 63, 601-614. [CrossRef]
- 21. Petropoulos SA; Fernandes, A.; Barros, L.; Ferreira, ICFR; Ntatsi, G. Morfologiczny, żywieniowy i chemiczny opis 'vatikiotiko', lokalnej lokalnej rasy cebuli z Grecji. Chemia Spożywcza 2015,182, 156-163. [CrossRef]
- 22. Liguori, L.; Adiletta, G.; Nazzaro, F.; Fratianni, F.; Di Matteo, M.; Albanese, D. Biochemiczne, właściwości przeciwutleniające i aktywność przeciwdrobnoustrojowa różnych odmian cebuli w rejonie Morza Śródziemnego. J. Pomiar żywności. Charakter. 2019,13, 1232-1241. [CrossRef]
- 23. Ej, KS; Szczupak, L.; Crosby, K.; Jones, R.; Leskovar, D. Różnice w ostrości cebuli ze względu na odmiany, środowisko wzrostu i rozmiary cebul. Nauka. Hortic. 2006,110, 144-149. [CrossRef]
- 24. Beesk, N.; Perner, H.; Schwarz, D.; Jerzy E.; Kroh, LW; Rohn, S. Rozmieszczenie kwercetyny-3'-O-diglukozydu, kwercetyny-4'-O-monoglukozydu i kwercetyny w różnych częściach cebuli (Allium cepa L.) pod wpływem genotypu. Chemia Spożywcza 2010,122, 566-571. [CrossRef]
- 25. Caruso, G.; Conti, S.; Villari, G.; Borrelli, C.; Melchionna, G.; Minutolo, M.; Russo, G.; Amalfitano, C. Wpływ czasu przesadzania i gęstości roślin na plon, jakość i zawartość przeciwutleniaczy cebuli (Allium cepa L.) w południowych Włoszech. Nauka. Hortic. 2014,166, 111-120. [CrossRef]
- 26. Perez-Gregorio, MR; Regueiro, J.; Simal-Gandara, J.; Rodrigues, AS; Almeida, DPF Zwiększanie wartości dodanej cebuli jako źródła flawonoidów przeciwutleniających: krytyczny przegląd. Crit. Rev. Food Sci. Nutr. 2014, 54,1050-1062. [CrossRef] [PubMed]
- 27. Pohnl, T.; Schweiggert, RM; Carle, R. Wpływ metody uprawy i doboru odmian na rozpuszczalne węglowodany i ostre zasady w cebuli (Allium cepa L.). J. Rolnictwo. Chemia Spożywcza 2018, 66, 12827-12835. [CrossRef] [PubMed]
- 28. Tedesco, I.; Węgiel, V.; Spagnuolo, C.; Minasi, P.; Russo, GL Identyfikacja i oznaczanie ilościowe flawonoidów z dwóch południowych włoskich odmian Allium cepa L., Tropea (cebula czerwona) i Montoro (cebula miedziana) oraz ich zdolność do ochrony ludzkich erytrocytów przed stresem oksydacyjnym. J. Rolnictwo. Chemia Spożywcza 2015, 63, 5229-5238. [CrossRef]
- 29. Villano, C.; Esposito, S.; Carucci, F.; Frusciante, L.; Carputo, D.; Aversano, R. Wysokoprzepustowe genotypowanie cebuli ujawnia strukturę różnorodności genetycznej i informacyjne SNP przydatne w hodowli molekularnej. Mol. Rasa. 2019, 39, 5. [CrossRef]
- 30. Mercati, F.; Longo, C.; Poma, D.; Araniti, F.; Lupini, A.; Mammano, MM; Fiorego, MC; Abenavoli, MR; Sunseri, F Genetyczna odmiana włoskiego pomidora o długim okresie przydatności do spożycia (Solanum lycopersicum L.) zbiór z wykorzystaniem SSR i cech morfologicznych owoców. Genet. Zasob. Przytnij Evol. 2014, 62, 721-732. [CrossRef]
- 31. Gonzalez-Perez, S.; Mallor, C.; Garces-Claver, A.; Merino, F.; Taboada, A.; Rivera, A.; Pomar, F.; Perovic, D.; Silvar, C. Odkrywanie różnorodności genetycznej i cech jakościowych w zbiorze cebuli (Allium cepa L.) Landrace z północno-zachodniej Hiszpanii. Genetyka 2015, 47, 885-900. [CrossRef]
- 32. Lotti, C.; Iovieno, P.; Centomani, I.; Marcotrigiano, AR; Fanelli, V.; Mimiola, G.; Summo, C.; Pavan S.; Ricciardi, L. Genetyczna, bioagronomiczna i żywieniowa charakterystyka jarmużu (Brassica oleracea L. var. bezgłowia) różnorodność w Apulii w południowych Włoszech. Różnorodność 2018,10, 25. [CrossRef]
- 33. Bardaro, N.; Marcotrigiano, AR; Bracuto, V.; Mazzeo, R.; Ricciardi, F.; Lotti, C.; Pavan S.; Ricciardi, L. Genetyczna analiza odporności na Orobanche crenata (Forsk.) w grochu (Pisum sativum L.) linia niskostrigolaktonowa. J. Pathol Roślin. 2016, 98, 671-675.
- 34. Wako, T.; Tsukazaki, H.; Yaguchi, S.; Yamashita, K.; Ito, S.; Shigyo, M. Mapowanie loci cech ilościowych dla czasu pośpiechów w gronach cebuli (Allium fistulosum) L.). Eufityka 2016, 209, 537-546. [CrossRef]
- 35. Dhaka, N.; Mukhopadhyay, A.; Paritosz K.; Gupta, V.; Pental, D.; Pradhan, AK Identyfikacja genowych SSR i konstrukcja mapy połączeń opartej na SSR w Brassica juncea. Eufityka 2017, 213, 15. [CrossRef]
- 36. Anandhan, S.; Mote, SR; Gopal, J. Ocena tożsamości odmianowej cebuli za pomocą markerów SSR. Nasiona Sci. Technol. 2014, 42, 279-285. [CrossRef]
- 37. Mitrova, K.; Swoboda, P.; Ovesna, J. Dobór i walidacja zestawu markerów do różnicowania odmian cebuli z Czech. Czech J. Genet. Rasa roślin. 2015, 51, 62-67. [CrossRef]
- 38. Di Rienzo, V.; Miazzi, MM; Fanelli, V.; Sabetta, W.; Montemurro, C. Ochrona i charakterystyka bioróżnorodności apulijskiej plazmy zarodkowej oliwek. Acta Hortic. 2018,1199,1-6. [CrossRef]
- 39. Mallor, C.; Arnedo-Andres, A.; Garces-Claver, A. Ocena różnorodności genetycznej języka hiszpańskiego Allium cepa Landrace do hodowli cebuli z wykorzystaniem markerów mikrosatelitarnych. Nauka. Hortic. 2014,170, 24-31. [CrossRef]
- 40. Rivera, A.; Mallor, C.; Garces-Claver, A.; Garcia-Ulloa, A.; Pomar, F.; Silvar, C. Ocena różnorodności genetycznej cebuli (Allium cepa L.) rasy z północno-zachodniej Hiszpanii i porównanie ze zmiennością europejską. NZJ Crop Hortic. 2016, 44, 103-120. [CrossRef]
- 41. De Giovanni, C.; Pavan S.; Taranto, F.; Di Rienzo, V.; Miazzi, MM; Marcotrigiano, AR; Mangini, G.; Montemurro, C.; Ricciardi, L.; Lotti, C. Genetyczna odmiana globalnej kolekcji plazmy zarodkowej ciecierzycy (Cicer arietinum L.) w tym akcesje włoskie zagrożone erozją genetyczną. Fizjol. Mol. Biol. Rośliny 2017, 23, 197-205. [CrossRef]
- 42. Mazzeo, R.; Morgese, A.; Sonnante, G.; Zuluaga, DL; Pavan S.; Ricciardi, L.; Lotti, C. Różnorodność genetyczna w rabe brokułów (Brassica rapa L. subsp. Sylvestris (L.) Janch.) z południowych Włoch. Nauka. Hortic. 2019, 253, 140-146. [CrossRef]
- 43. Jakse, M.; Marcina, W.; McCallum, J.; Havey, M. Polimorfizmy pojedynczych nukleotydów, indele i proste powtórzenia sekwencji do identyfikacji odmian cebuli. J. Am. Soc. Hortic. Nauka. 2005,130, 912-917. [CrossRef]
- 44. McCallum, J.; Thomson, S.; Pither-Joyce, M.; Kenel, F. Analiza różnorodności genetycznej i rozwój markera polimorfizmu pojedynczego nukleotydu w uprawnej cebuli cebulowej w oparciu o ekspresyjne znaczniki sekwencji - proste markery powtórzeń sekwencji. J. Am. Soc. Hortic. Nauka. 2008,133, 810-818. [CrossRef]
- 45. Baldwin, S.; Pither-Joyce, M.; Wright, K.; Chen, L.; McCallum, J. Opracowanie solidnych genomowych prostych markerów powtórzeń sekwencji do oceny różnorodności genetycznej w obrębie cebuli cebulowej i między nią (Allium cepa L.) populacje. Mol. Rasa. 2012, 30, 1401-1411. [CrossRef]
- 46. DeWoody, JA; Honeycutt, RL; Skow, LC Microsatellite markery z jelenia białoogonowego. J. Hereda. 1995, 86, 317-319. [CrossRef] [PubMed]
- 47. Khodadadi, M.; Hassanpanah, D. Irańska cebula (Allium cepa L.) odpowiedzi odmian na depresję wsobną. Świat Appl. Nauka. J. 2010,11, 426-428.
- 48. Abdou, R.; Bakasso, Y.; Saadou, M.; Baudoin, JP; Hardy, OJ Genetyczna różnorodność cebuli Nigru (Allium cepa L.) oceniane za pomocą prostych markerów powtórzeń sekwencji (SSR). Acta Hortic. 2016,1143, 77-90. [CrossRef]
- 49. Pavan S.; Lotti, C.; Marcotrigiano, AR; Mazzeo, R.; Bardaro, N.; Bracuto, V.; Ricciardi, F.; Taranto, F.; D'Agostino, N.; Schiavulli, A.; i in. Wyraźny klaster genetyczny w uprawnej ciecierzycy, jak ujawniono dzięki odkryciu i genotypowaniu markerów w całym genomie. Genom roślinny 2017, 2017,10. [CrossRef]
- 50. Pavan S.; Marcotrigiano, AR; Ciani, E.; Mazzeo, R.; Zonno, V.; Ruggieri, V.; Lotti, C.; Ricciardi, L. Genotypowanie przez sekwencjonowanie melona (Cucumis melo L.) pobranie plazmy zarodkowej z wtórnego centrum różnorodności uwydatnia wzorce zmienności genetycznej i cechy genomowe różnych puli genów. Genom BMC. 2017, 18, 59. [CrossRef]
- 51. Di Rienzo, V.; Sion, S.; Taranto, F.; D'Agostino, N.; Montemurro, C.; Fanelli, V.; Sabetta, W.; Boucheffa, S.; Tamendjari, A.; Paskwalon, A.; i in. Przepływ genetyczny wśród populacji oliwek w basenie Morza Śródziemnego. rówieśnik J. 2018, 6. [CrossRef]
- 52. Pasterz, LD; McLay, TG Dwa protokoły w mikroskali do izolacji DNA z tkanki roślinnej bogatej w polisacharydy. J. Plant Res. 2011,124, 311-314. [CrossRef]
- 53. Doyle, JJ; Doyle, JL Izolacja DNA roślinnego ze świeżej tkanki. Skupiać 1990,12, 13-14.
- 54. Kuhl, JC; Cheung, F.; Qiaoping, Y.; Marcina, W.; Zewdie, Y.; McCallum, J.; Katanach, A.; Rutherford, P.; zlew, KC; Jenderek M.; i in. Unikalny zestaw 11,008 znaczników sekwencji ulegających ekspresji w cebuli ujawnia ekspresję sekwencji i różnice genomowe między rzędami jednoliściennych szparagów i wiechlinowatych. Komórka roślinna 2004,16, 114-125. [CrossRef]
- 55. Kim, HJ; Lee, HR; Hyun, JY; Pieśń, KH; Kim, KH; Kim, JE; Hur, CG; Harn, CH Rozwój markerów do testowania czystości genetycznej cebuli przy użyciu SSR Finder. Koreańska rasa J.. Nauka. 2012, 44, 421-432. [CrossRef]
- 56. Schuelke, M. Ekonomiczna metoda znakowania fluorescencyjnego fragmentów PCR. Nat. Biotechnologia. 2000, 18, 233-234. [CrossRef] [PubMed]
- 57. Peakall, R.; Smouse, PE GenAlEx 6.5: Analiza genetyczna w Excelu. Oprogramowanie genetyki populacji do nauczania i badań: aktualizacja. Bioinformatyka 2012, 28, 2537-2539. [CrossRef] [PubMed]
- 58. Kalinowski ST; stożek, ML; Marshall, TC Zmiana sposobu, w jaki program komputerowy CERVUS uwzględnia błąd genotypowania, zwiększa sukces w ustalaniu ojcostwa. Mol. Ek. 2007,16, 1099-1106. [CrossRef]
- 59. Pritchard, JK; Stephens, M.; Rosenberg, NA; Donnelly, P. Mapowanie asocjacji w populacjach ustrukturyzowanych. Jestem. J. Hum. Genet. 2000, 67, 170-181. [CrossRef]
- 60. Evanno, G.; Regnaut, S.; Goudet, J. Wykrywanie liczby skupisk osób za pomocą oprogramowania STRUKTURA: badanie symulacyjne. Mol. Ek. 2005,14, 2611-2620. [CrossRef]
- 61. Earl, D.; VonHoldt, B. HARVESTER STRUCTURE: Strona internetowa i program do wizualizacji wyników STRUCTURE i wdrażania metody Evanno. Zachowaj. Genet. Zasob. 2011, 4. [CrossRef]
- 62. Takezaki, N.; Nei, M.; Tamura, K. POPTREEW: Internetowa wersja POPTREE do konstruowania drzew populacyjnych na podstawie danych o częstości alleli i obliczania innych wielkości. Mol. Biol. Ewol. 2014, 31, 1622-1624. [CrossRef]
- 63. Kumar S.; Stecher, G.; Li, M.; Knyaz, C.; Tamura, K. MEGA X. Molecular Evolutionary Genetics Analysis na różnych platformach obliczeniowych. Mol. Biol. Ewol. 2018, 35, 1547-1549. [CrossRef]